Woher kam die SARS-CoV-2 Omikron Variante?
Eine spannende Studie zeigt einen möglichen Ursprung von Omikron in Nagetieren auf. Andere vermuten einen Zusammenhang mit immunkomprimierten HIV-Patienten. Es ist unklar, ob die Ungewissheit sich komplett auflösen lässt. Eines ist jedoch ist sicher: Die westliche Vernachlässigung der öffentlichen Gesundheit in Entwicklungsländern ist ein historisches Problem mit weltweiten Folgen.
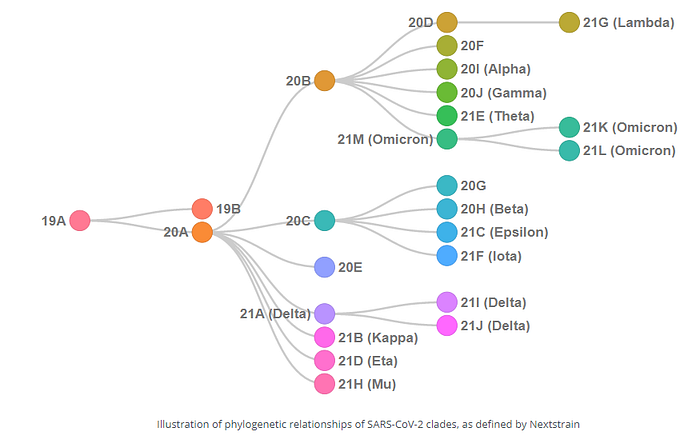
Seit die hochansteckende SARS-CoV-2 Variante B.1.1.529, heute Omikron, im frühen November in Gauteng, Südafrika entdeckt wurde, bereitete sie sich wie ein Lauffeuer um die Welt aus. Selbst in Ländern die momentan noch mit einer starken Delta Welle zu kämpfen haben übernimmt Omikron Variante einen immer größeren Anteil aller Neuinfektionen. In anderen Ländern ist Omikron schon längst der praktisch alleinige Verursacher von Covid-19.
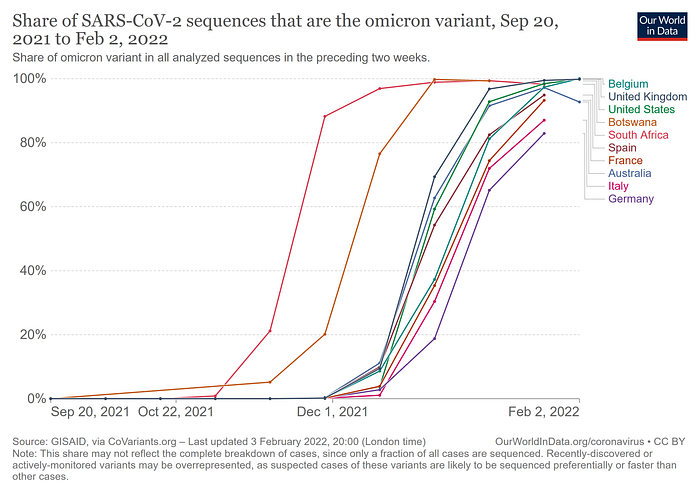
Nach zwei Jahren Pandemie scheint die Fähigkeit des Viruses, uns mit neuen Varianten zu überraschen, kaum abgenommen zu haben. Woher kommen ständig diese neuen Varianten und was macht Omikron so anders als Bisherige? Ein Team von Wissenschaftlern rund um Weifeng Qian, Professor für Genetik an der Universität der chinesischen Akademie der Wissenschaften in Peking, lieferten nun eine überzeugende Hypothese.
Die tierischen Ursprünge von Omikron?
Schon früh nach Entdeckung der Omikron Variante offerierten Wissenschaftler drei potentielle Ursprungszenarien (die NZZ berichtete); einerseits eine ‘versteckte’ Ausbreitung in einer Bevölkerungsgruppe ohne genomische Beobachtungsinfrastruktur, zweitens eine chronische Infektion in immunkomprimierten Patienten dessen Immunsystem über Monate den Virus nicht loswerden kann, und zuletzt eine vom Menschen infizierte Tierpopulation, die das Virus kultivierte und schließlich wieder auf den Menschen zurückübertrug.
Diesen letzten Punkt griffen Wenfang Qian und sein Team auf, und suchten in den viralen Genomen von Omikron nach Anhaltspunkten eines tierischen Wirtes.
Die Wissenschaftler konzentrierten sich auf hauptsächlich auf die vielen Mutationen, die die ersten gefundenen Omikron Sequenzen im Vergleich zur Ursprungsvariante von SARS-CoV-2, und späteren Omikron Genomen unterscheiden. Genauer, sie untersuchten, ob es gewisse Muster im ‘Mutationsspektrum’ gab zwischen den frühsten Sequenzen (‘welche gerade aus den Wirtstieren gesprungen sein könnten’) und späteren Omikron Genomen (‘alle Sequenzen bezogen nach dem 15. November’) gab, als die erste Welle sich in Südafrika ausbreitete und weitere de novo Mutationen anhäufte.
Mutationspektren beschreiben eine Nukleotidpräferenz von de novo Mutationen. Da RNA aus 4 Nukleotidbasen besteht (A, C, G, U), besteht in der Theorie eine Chance von ~33%, das z.B. aus einem A ein C wird. Praktisch ist es jedoch komplizierter, da Mutationen vielen zellinternen und externen Prozessen unterliegen, die charakteristische chemische Konsequenzen nach sich ziehen. So ist zum Beispiel eine ‘C zu U Transition’ oft ein Anzeichen für RNA Editierungsprozesse aufgrund einer Cytosin Deaminierung. Diese Deaminierung wiederum kann vermehrt durch z.B. UV-Licht ausgelöst werden. Andere Mutationspräferenzen wurden auch in Relation zu Tabak-Rauchen gefunden. In der Krebsforschung sucht man schon seit Jahren vermehrt nach diesen ‘Mutationsprofilen’ oder ‘mutational signatures’ als quasi molekulare Fingerabdrücke für krebsauslösende Substanzen und Einflüsse. Doch wie sieht das bei Viren aus?
In einer vorhergehenden Publikation konnte das Team rund um Wenfeng Qian zeigen, dass de novo Mutationen in SARS-CoV-2 sehr stark vom zellulären Umfeld des Wirtsorganismus bestimmt sind, und nicht so sehr vom Virus (und dessen Replikationsmachinerie) selbst abhängen. So aufgestellt fanden sie zu ihrer Überraschung in frühen Omikron Sequenzen ein Mutationsspektrum welches weder mit späteren Omikron Spektren, noch mit der generellen Verteilung der de novo Mutationen in SARS-CoV-2 vergleichbar sind. Späte Omikron Sequenzen deckten sich jedoch mit den generellen Mutationspräferenzen von SARS-CoV-2, verdeutlichen also einer Selektion im Menschen.
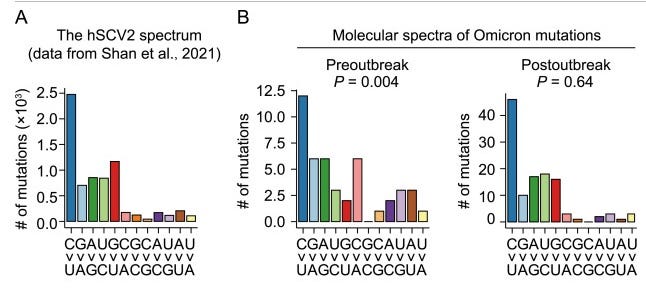
Nun ist eine statistische Abweichung zuerst mal kurios, aber längst noch kein schlüssiges Argument für einen tierischen Wirt. Die Wissenschaftler mussten tiefer graben. Im nächsten Schritt wandten sie sich also Coronaviren zu, welche aus verschiedenen Säugetierarten isoliert wurden. Sie erstellten phylogenetische Familienstammbäume für jede Tierfamilie, um daraus dann Rückschlüsse auf akquirierte de novo Mutationen zu ziehen und schlussendlich Mutationsspektren für individuelle Tierhintergründe zu generieren. Die breite Menge an verschiedensten Mutationsspektren wurde dann in einem Datensatz aggregiert und mithilfe von computerunterstützten Clustermethoden visualisiert. Nach dem Prinzip ‘gleich und gleich gesellt sich gern’ konnten die Wissenschaftler so feststellen, dass Mutationsspektren vom gleichen Wirtstierhintergrund viel besser zueinander passten als zu Spektren von anderen Wirtstieren. Durch diese grobe ‘Navigationskarte’ der Mutationsspektren konnten die Wissenschaftler danach aufzeigen, dass Coronaviren in Nagetieren (getestet: Mäuse) sehr ähnliche Mutationsmuster aufweisen als die frühen (jedoch nicht späteren) Omikron Genome.
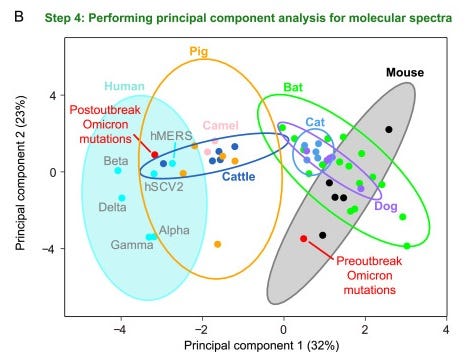
“Wir sind ziemlich sicher, dass Omikron sich nicht im Menschen entwickelt hat”, erläutert Weifang Qian auf Nachfrage. Er glaube Mäuse seien ein guter Kandidat, aber die genaue Wirtspezies können er nicht konklusiv bestätigen, dafür sei die momentane Auflösung der Mutationsspektren nicht hoch genug.
Jedoch ist Qian in seinem Glauben an Nagetiere nicht allein. Andere Wissenschaftler haben beobachtet, dass charakteristsiche Mutationen wie Q498R/H oder N501Y in dem viralen Spike Protein von Omikron den Tropismus zu Nagetieren erhöhen. Im Gegensatz zu Omikron (aber auch z.B. der Alpha Variante aus Großbritannien) können SARS-CoV-2 und die Delta Variante Mäuse und Ratten nicht infizieren. Eine kürzliche Studie bestätigt außerdem, dass diese charakteristischen Mutationen eine dramatisch erhöhte Bindungskraft zu Zelleintrittsrezeptoren von Ratten aufweisen. Andere Wissenschaftler wiederum fanden Spuren von diesen charakteristischen Mutationen in Abwasserüberprüfungen von New York City, Monate bevor Omikron existierte. Obwohl sie die Ursprünge dieser Sequenzen nicht nachverfolgen konnten, vermuteten die Wissenschaftler stark einen tierischen Ursprung, unter anderem in Ratten. Folgeexperimente zeigten, dass diese kryptischen Linien mit Omikron-ähnlichen Mutationen in der Lage waren, Zellen mit Maus- und Ratten-ACE2 effizient zu transduzieren. Könnte dies ein Zeichen konvergenter Evolution sein?
Ratten als Krankheitsüberträger sind in der Geschichte wohl bekannt, doch wie genau passen sie ins Bild von Omikron?
Von Ratten und Menschen
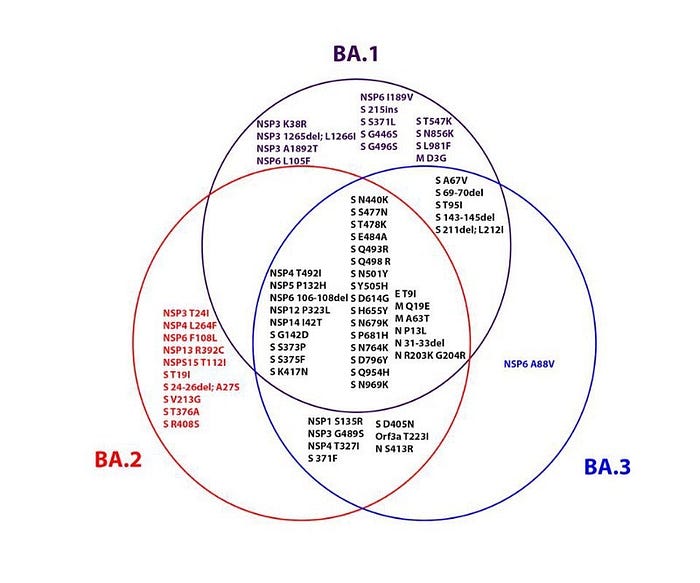
Wir besitzen keine eindeutigen epidemiologischen Daten zu den Ursprüngen von Omikron. Die ersten bestätigten Omikron Fällen wurden von der WHO retrospektiv auf den 9. November datiert; jedoch vermuten Wissenschaftler aufgrund des S-Gen Dropouts in PCR Tests, dass zu diesem Zeitpunkt Omikron schon Delta als dominante Variante abgelöst hatte. Eine kürzlich veröffentlichte Nature Studie aus Südafrika zeigt außerdem auf, dass bis Ende November drei evolutionär verwandte, aber unabhängige Omikron Linien (BA.1, BA.2, BA.3) in der Provinz Gauteng, Südafrika grassierten. Modellierungen gehen mit einem Startzeitpunkt für Mensch-zu-Mensch Infektionsketten mit Omikron im frühen Oktober einher.

Ob die Provinz Gauteng, mit der Großstadt Johannesburg, wirklich den Ort des zoonotischen Übersprungs darstellte, oder einfach nur ein Epizentrum der Infektionen, lässt sich schwer eindeutig nachweisen.
Wenn uns das SARS-CoV-2 Virus eines gezeigt hat, dann das es dazu fähig ist, in verschiedenste Tiere zu springen. Von exotischen Marderhunden, Zibetkatzen oder Gürteltieren bis zu Nerzen, Frettchen oder Hirsche, ob Haustiere, Zootiere oder Wildtiere, unsere menschliche Inkompetenz das Virus einzudämmen hat mittlerweile viele andere Tiere, mit denen wir Kontakt pflegen, betroffen. Zoonotische Sprünge zwischen Tieren und Menschen benötigen vor allem eines: viele Gelegenheiten. Im Umkehrschluss bedeutet dies, dass die Wahrscheinlichkeit eines zoonotischen Rücksprungs vom Tier zum Menschen dann gegeben ist, wenn eine dementsprechend große Tierpopulation erstmal den Virus zirkuliert, und der Mensch viel in Kontakt mit diesen Tieren steht. Ratten in dichten Städten scheinen dafür prädestiniert.
Diesen Gedanken verfolgten auch belgische Wissenschaftler, die nach einer SARS-CoV-2 Welle in der Stadt Antwerpen schon im November 2020 Ratten auf potentielle Infektionen testeten, jedoch keine Evidenz dafür fanden. Eine weitere Studie aus Hong Kong im February 2021 fand auch keine direkte Evidenz für akute Infektionen, jedoch hatte eines der 213 getesten Tiere spezifische Antikörper gegen SARS-CoV-2, welche nicht auf andere zirkulierende Alphacoronaviren zurückzuführen sei. Zum Studienzeitpunkt (und bis heute) gab es in Hong Kong jedoch verhältnismäßig wenige SC2 Infektionen gesamt.
Im Gegensatz zum gepflegten Antwerpen oder dem pandemieresitenten Hong Kong sieht die Lage in anderen Ländern wesentlich dramatischer aus. So infizierten sich in Johannisburg zum Beispiel ein Drittel aller Einwohner schon in der ersten Welle, zufällig zu jenem Zeitpunkt wo phylogenetische Analysen den letzte gemeinsame Vorfahre von Omikron vermuten. Zusätzlich befindet sich Johannisburg seit Jahrzehnten in einer öffentlichen Gesundheitskrise ausgelöst durch Ratten. Studien fanden Rattenbefall in über 50% aller Haushalte; vor allem Haushalte in ärmeren Townships, wo Abwasserreinigung und Müllentsorgung historisch problematisch ist, berichten von dramatischen Belastungen der Anwohner durch Ratten.

Könnte ein solches Umfeld die richtigen Voraussetzungen für zoonotische Sprünge schaffen?
Weifeng Qian denkt ähnlich. “Ich halte es für durchaus möglich, dass auch Ratten ein wahrscheinlicher Wirtorganismus für Omikron gewesen sein könnte, um dort Mutationen anzusammeln. Ursprünglich hatte unsere Studie den breiteren Titel ‘Nagetiere’ [englisch ‘rodents’] geplant, aber wir hatten nicht wirklich Evidenz für andere Nagetiere als Mäuse”.
Dr. Jacqueline Weyer vom Center for Emerging Zoonotic and Parasitic Diseases (CEZPD) in Südafrika sagt, dass es derzeit keine Überwachungsprogramme bei Nagetieren für SARS-CoV-2 gibt, da diese bisher keine wissenschaftliche Begründung fanden. Übertragungen von Mensch zu Mensch sei bei Weitem der vorherrschende Übertragungsweg für SC2 in Südafrika. Während es gelegentliche Infektionsübersprünge auf Tiere gibt, haben sie noch keine Anhaltspunkte für anhaltende Übertragung von SC2 in Tierpopulationen. Eine Infektionsstudie an Mäusen zeigte jedoch, dass grundsätzlich ein hohes Potenzial für eine anhaltende Übertragungen von SARS-CoV-2 zwischen Nagetier zu Nagetier besteht.
Wie eine virale Übertragung zurück auf den Menschen funktionieren könne, sehe man an anderen, von Nagetieren stammende, Roboviren, z.B. Hantavirus oder Arenaviren, diese würden normalerweise durch Rattenausscheidungen übertragen. Sporadische zoonotische Sprünge von Roboviren zu Menschen treten auf, führen aber in der Regel nicht zu einer weiteren Übertragung von Mensch zu Mensch. Ob das respiratorische SARS-CoV-2 den Weg von der Ratte zurück in den Menschen schaffen könne ist bisher unklar.
Lourens Swanepoel von der Universität Venda glaubt, dass es „definitiv genug Begegnungen zwischen Nagetieren und Menschen gibt, um eben solche Gelegenheiten für zoonotische Übertragungen zu bieten“, aber seine Arbeit konzentriert sich hauptsächlich auf ländliche Gebiete, in denen einheimische Mäusearten vorherrschen.
Professorin Amanda Bastos von der University of Pretoria, Südafrika, beschäftigt sich seit Jahren mit zoonotischen Risiken durch Ratten. Je nach Erreger seien mehrere Übertragungswege bei Ratten möglich. Von Rattenkot über gemeinsame Nahrungsquellen bis hin zu direkten Angriffen. Sie wies ferner darauf hin, dass lokale Medienberichterstattung in Südafrika darauf hindeutete, dass der Rattenbefall während der Pandemie erheblich zugenommen habe. „Höchstwahrscheinlich aufgrund des Rückgangs der Schädlingsbekämpfungsbemühungen während der Covid-Sperren zurückzuführen“, aber sie habe keine harten Zahlen dazu.
Wie präsent die Gefahr wirklich ist bedarf schlussendlich weiterer Studien. Die Tatsache, dass es bisher keine kostenintensiven genetischen Überwachungsprogramme in Hochrisikostädten gibt ist ebenso nachvollziehbar wie besorgniserregend.
Die mysteriöse Epidemiologie der Omikron Linien
Auch epidemiologisch fände ein zoonotischer Ursprung Omikron’s durchaus Unterstützung. Omikron hatte vom Beginn an bereits mehrere genetisch separierte Linien (genannt BA.1, BA.2 and BA.3). Die Tatsache, dass sich diese Omikron Schwesterlinien genetisch so stark unterscheiden ist kurios, da die Zeit zwischen ersten menschlichen Omikron Infektionen und dem Beobachten der verschiedenen Schwesterlinien eine so starke Diversifizierung voneinander schwer erklären kann. Dies suggeriert, dass entweder diese Aufspaltung der hochansteckenden Omicron Linien schon vor Monaten unbemerkt in Menschen passierte, oder wir beobachten mehrere Sprünge aus einem infizierten Tierreservoir.
So denkt auch Spyros Lytras, ein Doktorant am Zentrum für Virusforschung in Glasgow. Er sieht die verschiedenen gefundenen Unterlinien von Omikron schwer vereinbar mit einer chronischen Infektions-Erklärung in HIV Patienten. Die Tatsache, dass Omikron zuerst in Südafrika gefunden wurde, welches eine hervorragende Sequenzierungs-Infrastruktur besitzt und wohl den wichtigsten Reiseknotenpunkt für andere Gegenden Afrikas ohne genomische Beobachtung darstellt, überrascht ihn nicht. Zusammen mit der hohen Ungeimpften Rate in Afrika, hält er einen ‘unbeobachteten’ Ausbruch immer noch für eine ebenso wahrscheinliche Möglichkeit als dass Omikron aus einem Tierreservoir zurück in den Menschen gesprungen sei.
“Das Ermutigende an einem potentiellen tierischen Ursprung ist die Tatsache, dass wir ‘Vorgängersequenzen’ von Omikron immer noch finden könnten”, gibt er zu bedenken. Theoretisch könne also eine konklusive Antwort noch gefunden werden. Jedoch müssten wir schnell sein, denn irgendwann werde Omikron, welches konstant vom Menschen auf Tiere überspringt, diesen Hintergrund auch verwischen.
Ein Tierreservoir liefere außerdem eine gute Erklärung für die ungewöhnlichen Eigenschaften von Omikron, unter anderen einen anderen molekularen Zelleintrittsmechanismus. Eine Selektionsstudie der Omikron Mutationen, geleitet von Prof. Sergei Pond von der Temple Universität in Philadelphia, weist darauf hin, dass die vielen ungewöhnlichen Mutationen in Omikron die biologische Funktion des Spike Proteins so stärk verändern, dass sie eher einem Antigenshift als dem mehr graduierlichem Antigendrift gleiche.
In Influenzaviren werden graduelle Antigendrift-Mechanismen oft der Ausbreitung in Menschen zugeschrieben, während die dramatischeren Antigenshifts eher tierischen Reservoirs oder Rekombinationen mit anderen Viren zugeschrieben werden.

Die selbe Selektionsstudie zeigte jedoch auch, dass Omikron’s Mutationen individuell weniger ‘fit’ sind als die Grundsequenzen. Das die Mutationen in Kombination adaptiv zu sein scheinen lässt vermuten, dass sie fast gleichzeitig entstanden sein müssen. Sergei Pond ist sich weniger sicher, welche Faktoren dieses ‘gleichzeitigem Aufkommen’ begünstigen, aber er glaubt, dass irgendwann eine chronische Infektion beim Menschen wohl eine wichtige Rolle gespielt haben muss.
Was ist mit chronisch immunkomprimierten Patienten?
Viele Indizien zeigen die Wahrscheinlichkeit eines zoonotischen Ursprung der Omikron Variante auf. Weitere Klarheit könnten sowohl Infektionsstudien in Ratten, als auch genomische Untersuchungen in den relevanten Tierpopulationen schaffen.
Es ist aber eine andere Ursprungstheorie die momentan auf der Grundlage aktuellen Fakten möglicherweise besser erklären kann, wie sich bestimmte Merkmale von Omicron entwickelt haben könnten.
So hat zum Beispiel auch eine kürzlich veröffentlichte Fallstudie einer SARS-CoV-2 infizierten AIDS Patientin für Aufmerksamkeit gesorgt. Diese testete monatelang positiv für SARS-CoV-2, ohne das Virus loszuwerden, und musste aufgrund von Gesundheitsproblemen öfters in Krankenhaus. Die entnommenen Proben erlaubten Wissenschaftlern, die Evolution des SARS-CoV-2 Viruses rückwirkend nachzuverfolgen. Über Zeit notierten die Wissenschaftler eine Anhäufung von Mutationen, die dem Virus halfen, sowohl Ansteckungs- aus auch Vakzin-induzierten neutralisierenden Antikörpern zu entkommen. Einige dieser ‘Immunflucht’ Mutationen sind auch in Omikron vorhanden. Andere Fallstudien in HIV-Patienten finden auch Omikron-ähnliche Mutationen die die neutralisierende Wirkung von Antikörpern wohl umgehen.
Darüber hinaus zeigte eine Strukturstudie, dass sich das Spike-Protein in Omikron zu einer geschlosseneren physikalischen Konfiguration entwickelt hat, was für Forscher eine längere Exposition gegenüber einer antikörperbasierten Immunabwehr anzeigt. Schlussendlich weist das Verhältnis von nicht-synonymen zu synonymen (dN/dS) Mutationen, ein nützliches Maß zur Beurteilung des Selektionsdrucks, ebenfalls auf eine sehr starke positive Selektion von Omikrons-Mutationen hin.
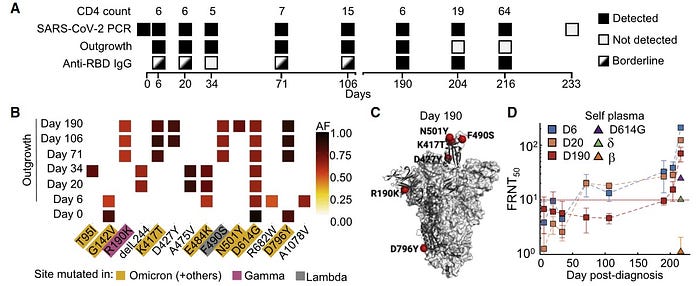
Genau diese Erkenntnisse machen es Prof. Andrew Rambaut von der University of Edinburgh schwer, sich vorzustellen, dass irgendein nichtmenschlicher Wirt oder eine Übertragung zwischen Gruppen überhaupt in der Lage ist, diese Mutationen hervorzubringen. Die virale Vielfalt in einem einzelnen chronisch infizierten Individuum viel höher ist als in einer Gruppe an Infizierten, da diese viralen Genome nicht durch eine reinigende Selektion zwischen Übertragungen „gesäubert“ werden. Andere Studien stimmen darin überein, dass Übertragungsengpässe zwischen Wirten für SC2 selbst bei ‘Superspreading’-Ereignissen sehr eng sind und die Virusentwicklung dramatisch verlangsamen. Einige Wissenschaftler postulierten sogar, dass ein Blick in chronisch infizierte Patienten einen Einblick in die zukünftige Entwicklung von Viren geben kann.
Andrew Rambaut glaubt, dass ein chronisch infizierter Patient die einzige zelluläre Umgebung sei, die einen so starken und anhaltenden Selektionsdruck überhaupt ausüben könne, diese hohe Anzahl immunevasiven Mutationen in Omikron hervorzubringen. Er weist auch darauf hin, dass sich SARS-CoV-2 kaum verändert hat, als es in Dänemark und den Niederlanden auf Nerze übersprang. Außerdem wurde gezeigt, dass die wenigen Mutationen, die in diesem tierischen Reservoir erworben wurden, die virale Fitness nicht erhöhten.
Christian Drosten vom Charité Berlin sieht jedoch ebendies als Zeichen gegen einen ‘chronischen’ Ursprung Omikrons, da die zusätzliche Last der Fluchtmutationen meistens mit anderen Veränderungen einhergehen, die die Infektionsfähigkeit beeinträchtigen können, wie es zum Beispiel bei chronischen Infektionen mit Grippeviren der Fall ist. “Diese [chronischen] Viren zeigen eine verringerte Fitness in der wirklichen Welt draußen’, gab er in einem Science Magazin Interview zu verstehen. Eine chronische Infektion sei weniger konsistent mit der erhöhten Ansteckungsfähigkeit von Omikron, aber ausschließen kann man es nicht. Das ist jedoch nicht der einzige Einwurf gegenüber einer chronischen Infektion’s Ursprungshypothese.
Der fast gleichzeitige Ausbruch mehrerer verwandter Omicron-Unterlinien ist epidemiologisch schwer mit einem einzigen menschlichen Wirt zu erklären. Da die drei Unterlinien sich zeitlich früh abtrennten und im Grunde schon entfernte Verwandte voneinander waren, als die ersten Omikron Ansteckungen stattfanden, müsste der chronisch infizierte Patient diese drei konkurrierenden Linien im selben Körper gehalten haben. Eine Art dynamische Pattsituation für Monate, in der sich in einem einzigen Körper drei verschiedene virale Unterlinien gegen das menschliche Immunsystem und gegeneinander entwickelten, ohne das eine ‘Siegerlinie’ die anderen verdrängt. Und während all diese interne Konkurrenz und der starke Selektionsdruck andauerten, schienen sowohl BA.1 als auch BA.2 einzigartige Wege gefunden zu haben, um auch die Übertragungskapazitäten zu erhöhen, um andere Hosts besser zu infizieren.
Während solch eine Szenario erstmals unglaublich klingt, gibt es wissenschaftlich nachgewiesene Präzedenzfälle für diese Dynamik bei anderen Virusinfektionen, zum Beispiel HIV-Superinfektionen. Diese superinfizierten Patienten, die mehrere HIV-Linien gleichzeitig beherbergen, können auch mehr als nur eine Viruslinie auf andere übertragen. Andrew Rambaut sieht in den frühen Berichten, dass die BA.2-Unterlinie jetzt BA.1 in mehreren Ländern ersetzt, ein mögliches Merkmal dieser gemeinsam entwickelten Dynamik.
Eine interessante Spekulation, doch bisher haben wir diese vorgeschlagene Dynamik mehrerer SARS-CoV-2-Linien weder bei HIV-Patienten oder anderen chronischen infektionen nicht beobachtet. Vermehrte Studien und Beobachtungen in immunkomprimierten Patienten könnte durchaus diese Hypothese bestätigen.
Schlussendlich müssen wir bedenken, dass alle vorgeschlagenen Hypothesen immer noch unter unvollständigen Daten leiden.
Deshalb kann auch eine ‘herkömmliche’ Selektion von Omikron in unbeobachteten Bevölkerungsgruppen, vor allem ländliche oder einkommensschwache soziale Gruppen ohne Zugang zu medizinischen Einrichtungen, zum jetzigen Zeitpunkt nicht komplett ausgeschlossen werden. Es ist jedoch fraglich, ob solche Gruppen den nötigen Selektionsdruck ausüben könnten, eine mutationsreiche Variante wie Omikron in relativ kurzer Zeit entstehen zu lassen. Außerdem lässt die lauffeuerartige Ausbreitung der verschiedenen Omikron Schwesterlinien, kurz nach Entdeckung in Südafrika, es offen, ob diese wirklich stillschweigend in anderen Ländern für Monate unbemerkt zirkulieren konnten.
Ob HIV-Patienten oder unbeobachtete Gruppen, eine reine Selektion in Menschen lässt sich mit den von Wenfeng Qian gefundenen nicht-menschlichen ‘Mutationsspektren’ der frühen Omikron Sequenzen schwer in Einklang bringen. Doch kann andererseits ein kurzer viraler Aufenthalt in einem Tierreservoir wirklich die schiere Anzahl dieser Immunflucht-Mutationen erklären? Zuletzt kann auch eine Kombination verschiedener menschlicher und tierischer Faktoren an dieser Stelle nicht ausgeschlossen werden.

Gerade wegen dieser Unklarheiten zögern viele Wissenschaftler noch immer, eine definitive Antwort auf die Frage nach der Herkunft von Omicron zu geben. Kristian Andersen, ein Forscher für Infektionskrankheiten am Scripps Research Institute in Kalifornien, tendierte lange zu einer „umgekehrten Zoonose“ Erklärung für Omicron, hält aber die aufkommenden Daten über eine starke positive Selektion bei HIV-Patienten für die derzeit überzeugendste Hypothese.
Alle, mit denen ich gesprochen habe, sind sich einig, dass es zu früh ist, die Tür für irgendein Szenario vollständig zu schließen. Vieles kann sich noch ändern, wenn neue Daten eintreffen. Schließlich ist Omicron erst wenige Monate alt und es wird in Zukunft mehr zu lernen geben, wenn man sich eingehender mit potenziellen Tierreservoirs und chronisch infizierten Patienten befasst.
Heute mögen die Ursprünge also immer noch ein Mysterium sein, aber wir können sicher sein, dass einige unserer klügsten Köpfe daran arbeiten.
Mit diesem Hinweis in die Zukunft würde normalerweise ein Artikel wie dieser enden. Allerdings komme ich nicht umhin, mich zu fragen, welche Lektionen Omikron uns wirklich schon heute beibringt?
Ein Warnsignal?
Wie so oft in dieser Pandemie der Unklarheiten gibt es auch bei den Ursprüngen Omikrons keine absolute Sicherheit. Ein roter Faden lässt sich jedoch in allen vorgeschlagenen Entstehungsszenarien ausmachen: Allen gemeinsam ist die jahrzehntelange Vernachlässigung der öffentlichen Gesundheit in Entwicklungsländern.
Omicron lehrt uns, dass städtische Rattenplagen, die AIDS-Pandemie oder der fehlende Zugang zu medizinischer Versorgung in Afrika leider mehr sind als nur ein lokales Problem in einer vernetzten Welt. Bei Viren kann aus einer lokalen oder entfernten Aufmerksamkeitslücke schnell eine globale Katastrophe werden.
Viele Berichte verurteilen zu Recht die ungleiche Verteilung von SARS-CoV-2-Impfstoffen weltweit. Derzeit warten in Afrika noch mehr als 1 Milliarde Menschen auf ihre erste Dosis, während in Europa und Nordamerika viele Auffrischungskampagnen nicht an der Verfügbarkeit von Wirkstoffen, sondern an der Bereitschaft zur Impfung scheitern.
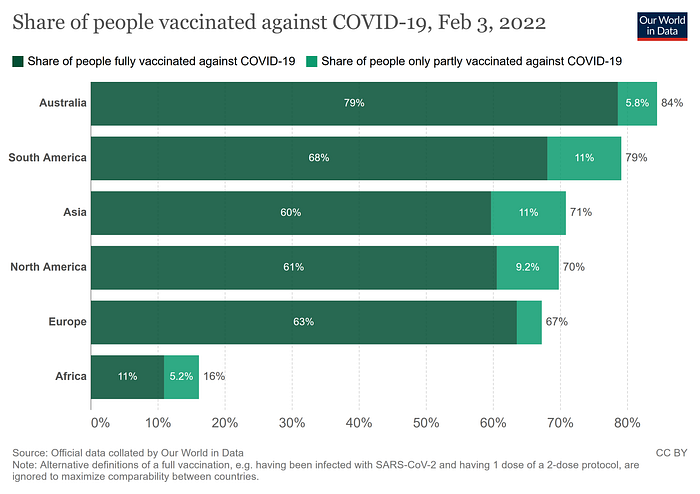
Impflücken sind auch für uns in entwickelten Ländern ein dramatisches Thema, da sie dem Virus mehr Chancen geben, Menschen schwer krank zu machen und auch kritische Mutationen zu sammeln. Die Regierungen fordern die Bürger zu Recht auf, diese „Impflücken“ zu schließen und es ist auch zunehmend über Impfmandate nachzudenken. Es ist Zeit zu handeln, auch wenn es politisch schwierig sein mag.
Auf noch weit weniger politischen Handlungsbedarf stößt das Mahnen vor ‘öffentlichen Gesundheitslücken’ anderer Nationen, obwohl nun mittlerweile jedem klar sein sollte, dass lebender Wildtierhandel und Massentierhaltung wohl kaum risikofreie Praktiken darstellen. Trotzdem hängt unsere Gesundheit unweigerlich mit der Völkergesundheit anderer Länder zusammen.
Die Entstehung von Omikron, wie auch die Pandemie selbst, zeigt auf, dass wir ‘öffentliche’ Gesundheit breiter denken müssen als die nationale Handhabung eines Krankheitserregers. Rattenplagen und AIDS wüten seit Jahrzehnten in afrikanischen Ländern. Südafrika’s überragendes genomisches Überwachungssystem ermöglichte es der Welt, vor Omicron gewarnt zu werden. Aber das ist nur eine Seite der Medaille. Echte Vorsorge erfordert eine verantwortungsbewusste globale Zivilisation, die afrikanische Nationen dabei unterstützt, Lebensumstände für ihre Bevölkerung zu schaffen, die das Risiko der Entwicklung solcher viraler Krankheitserreger von vornherein drastisch reduzieren. Bisher haben wir nicht einmal die grundlegendsten Interventionen geschafft, zum Beispiel eine vorübergehende Aufhebung der Patentbeschränkungen für die Covid-Impfstoffe, sodass andere Länder möglicherweise eine Chance haben, Impfungen nachzuholen. Wir brauchen schnell tiefgreifende Reformen.
SARS-CoV-2 wird endemisch werden. Wir werden wahrscheinlich nie in der Lage sein, zoonotische Übertragungen vollständig zu vermeiden oder die Virusweiterentwicklung komplett zu unterbinden. Das bedeutet jedoch nicht, dass wir machtlos sind. Wir können und sollten unnötige oder besonders riskante Umstände minimieren, wo immer sie auf der Welt auftreten. Angesichts unserer gegenwärtigen Vernachlässigung der Entwicklungsländer war die Entstehung von Omikron vermutlich unaufhaltbar.
Und doch sind wir nicht zur Wiederholung verdammt, wenn wir die Gegenwart als Zeit des Handelns begreifen.
Omikron wird nicht die letzte gefährliche SARS-CoV-2-Variante sein, mit der wir rechnen müssen. In einer vernetzten Welt voller unkluger Praktiken, Tierausbeutung und gravierender Lücken im Bereich der öffentlichen Gesundheit werden wahrscheinlich auch weitere zoonotische Pandemien dem Verlauf von SARS-CoV-2 folgen.
Bei all der momentanen Ungewissheit dieser Pandemie ist dies wohl die eine ernüchternde Klarheit, die uns die Wissenschaft schon heute geben kann.
Quellen:
- Kupferschmid Kai, Science, 2021
- Wei C. et al., Journal of Genetics and Genomics, 2021
- Barak Y. et al., J. Biol. Chem, 1995
- Chen Z. et al., BMC Cancer, 2020
- Shan K. et al., The Innovation, 2021
- Shuai H. et al., The Lancet, 2021
- Bate N. et al., biorxiv, 2021
- Smyth DS. et al., Nature, 2022
- Viana R. et al., Nature, 2022
- Colombo VC. et al., Transbound Emerg Dis., 2021
- Miot E. et al., Emerging Infectious Diseases, 2022
- George JA. et al., SAMJ, 2021
- Jassat W. et al., International Journal of Environmental Health Research, 2013
- Chelule PK. et al., Int J Environ Res Public Health, 2021
- Fagre A. et al., PLoS Pathog., 2021
- Martin DP. et al., biorxiv, 2022
- Dowdle WR. et al., Bull Pan Am Health Organ, 1976
- Cele S. et al., Cell Host & Microbe, 2022
- Riddell AC. et al., medrxiv, 2022
- Maponga TG. et al., SSRN, 2022
- Gobeil SMC. et al., biorxiv, 2022
- Kryazhimskiy S. et al., PLoS Genetics, 2008
- Morales AC. et al., Genome Biology and Evolution, 2021
- Braun KM. et al., PLoS Pathogens, 2021
- Hannon WW. et al., biorxiv, 2022
- Kemp SA. et al., Nature, 2021
- Oreshkova N. et al., Euro Surveill., 2021
- Zhu J. et al., Cell reports, 2022
- Gao Y. et al., Front Med., 2017
- Novitsky V. et al., PLoS One, 2016
